Bu makalede kalorimetrenin ne olduğu ve ne için kullanıldığı açıklanmaktadır. Ayrıca mevcut farklı kalorimetre türlerini ve bu ölçüm cihazının nasıl çalıştığını keşfedeceksiniz.
Kalorimetre nedir?
Kalorimetre , bir vücut tarafından alınan veya kaybedilen ısı miktarını ölçmek için kullanılan bir laboratuvar cihazıdır. Ek olarak kalorimetre, bir maddenin özgül ısısını belirlemek için kullanılan bir araçtır.
Örneğin, bir kimyasal reaksiyon sırasında açığa çıkan ısı formundaki enerjiyi ölçmek için bir kalorimetre kullanılabilir.
En modern kalorimetreler geniş bir sıcaklık aralığında çalışma kapasitesine sahiptir, bazıları 3500 K’ye ulaşabilir. Buna ek olarak, şu anda kalorimetreler çok hassastır, karakteristiklere ve sıcaklığa bağlı olmasına rağmen %1’den daha az bir doğruluğa sahip olabilirler. kalorimetre kullanımı.
Kalorimetride kalorimetrenin uygulamaları çoktur. Kalorimetreler biyolojik bir çalışma gerçekleştirmek, kalite kontrolü gerçekleştirmek ve hatta biyolojik hızı incelemek için kullanılabilir.
Kalorimetrenin parçaları
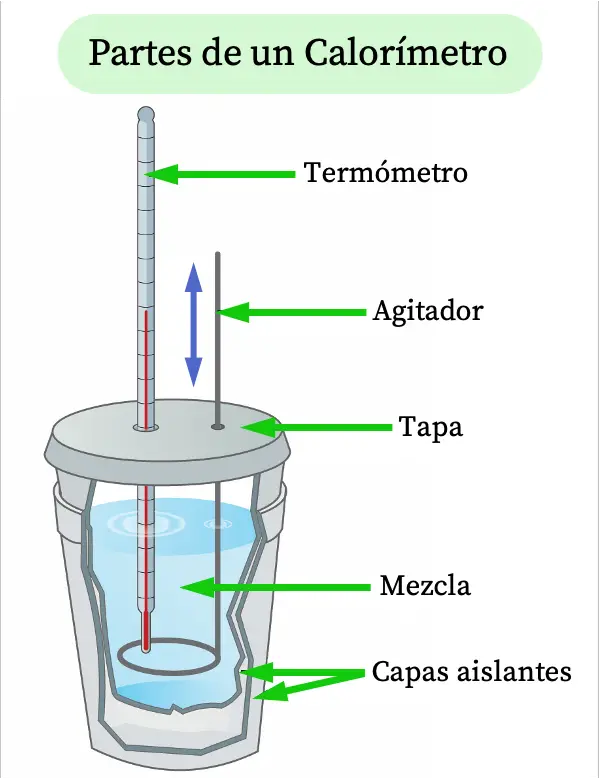
Kalorimetrenin tanımı dikkate alındığında tipik bir kalorimetrenin bölümleri aşağıda açıklanmaktadır:
- Termometre : Kalorimetrenin içindeki sıcaklığı ölçmenizi sağlar.
- Karıştırıcı : Kalorimetrenin karışımın sıcaklığını yükseltmek için sürekli karıştırılan kısmı.
- Kapak : Çalışılacak karışımın tanıtılması için açılıp kapatılabilen kapak.
- Karışım : Kalori analizi yapmak istediğimiz maddedir.
- Yalıtım katmanları : Kalorimetre kabı, ortamın sıcaklığının etkilememesi için karışımı dışarıdan termal olarak yalıtmalıdır. Bu nedenle genellikle polistiren olmak üzere iki kat ısı yalıtımından oluşurlar.
Kalorimetre türleri
Farklı kalorimetre türleri aşağıdaki gibidir:
- Adyabatik kalorimetre : Adyabatik kalorimetreler izole adyabatik reaksiyonları incelemek için kullanılır, yani dışarıyla ısı alışverişi gerçekleşemez. Bununla birlikte, bir miktar ısı her zaman kaybedilir, dolayısıyla telafi etmek için genellikle bir düzeltme faktörü uygulanır.
- Reaksiyon Kalorimetresi – Kapalı ve yalıtılmış kalorimetrenin içinde kimyasal bir işlem gerçekleşir. Genel olarak bir reaksiyonun açığa çıkardığı ısıyı belirlemek için kullanılır; sabit sıcaklık gerektiren reaksiyonlarda da kullanılır.
- Isı Akısı Kalorimetresi – Bu tipte, bir ısıtma/soğutma ceketi fiziksel sürecin sıcaklığını kontrol eder. Reaksiyon ısısı, ısı transfer akışkanı ile proses akışkanı arasındaki sıcaklık farkı ölçülerek belirlenir. Diğer kalorimetre türlerine göre daha az hassastırlar.
- Isı dengesi kalorimetresi : Bu tip kalorimetre ayrıca proses sıcaklığını kontrol etmek için bir ısıtma/soğutma ceketi gerektirir. Isı, transfer akışkanının kazandığı veya kaybettiği ısının izlenmesiyle ölçülür.
- Enerji Kompanzasyonlu Kalorimetre : Bu durumda sabit bir sıcaklığı korumak için kaba eklenen bir ısıtıcı kullanılır. Isıtma enerjisi reaksiyonun ihtiyaçlarına göre ayarlanabilir.
- Sabit Akışlı Kalorimetre – Bu tip kalorimetre, kabın duvarından sabit bir ısı akışı sağlar.
- Bomba Kalorimetresi : Bu tip kalorimetre yanma ısısını hesaplamak için kullanılır. Yakıtı tutuşturmak için bir elektrik kıvılcımının uygulanması yaygındır. Ayrıca çok yüksek basınçlarda çalışırlar.
- Calvet tipi kalorimetre : Bu kalorimetreler 3 boyutlu bir akış sensörü kullanır. Büyük numune boyutları için çok uygundurlar çünkü daha büyük bir reaksiyon kabı boyutunun kullanılmasına izin verirler.
- Sabit Basınçlı Kalorimetre : Bu tip kalorimetre, sabit basınç altındaki bir çözeltideki ısı değişimini ölçmek için kullanılır.
- Diferansiyel Taramalı Kalorimetre – Genellikle iki tepsi vardır, bir numune tepsisi ve bir referans tepsisi. Referans tepsisi boş kalırken numune tepsisinde numune bulunur. Her kap ayrı ayrı belirli bir oranda ısıtılır ve bu oran deney boyunca korunur. Ancak bir bilgisayar sistemi her tavanın aynı oranda ısınmasını sağlar, böylece ölçüm yapılabilir. Numune tepsisinin altındaki ısıtıcının boş referans tepsisine göre daha fazla çalışması gerekir, bu da daha fazla ısı ürettiği anlamına gelir. Böylece kalorimetre, tepsilerde yayılan ısı miktarındaki farka göre ölçüm yapar.
- İzotermal Titrasyon Kalorimetresi – Bu tipte reaksiyonun ısısı bir titrasyon deneyini izlemek için kullanılır. Reaksiyonun orta noktasını, entalpisini ve bağlanma afinitesini belirlemek mümkündür. Bu tip kalorimetre, ilaç endüstrisinde potansiyel ilaç adaylarını sınıflandırmak için çok faydalıdır.
Kalorimetre nasıl çalışır?
Önceki bölümde gördüğünüz gibi kalorimetrelerin pek çok türü vardır ve her biri farklı şekilde çalışır. Aşağıda laboratuvar deneylerinde en çok kullanılan adyabatik kalorimetrenin nasıl kullanıldığı açıklanmaktadır.
Kalorimetrenin çalışması çalkalayıcının sallanmasıyla bağlantılıdır. Çalkalayıcıyı kullanmadan önce numuneyi kalorimetreye yerleştirmek mantıklıdır. Numuneyi izole etmek için kapak kapatıldığında karıştırıcının hızlı bir şekilde hareket ettirilmesi gerekir, dolayısıyla numunenin sıcaklığı artacaktır. Termometre ile numunenin hangi sıcaklıkta olduğunu görebilirsiniz.
Daha sonra numune çalkalandıktan sonra ilgili ölçümler gerçekleştirilir. Böylece sonuçlar numuneyi ısıtmadan önce ölçülen verilerle karşılaştırılabilir. Ve deney sırasında toplanan tüm verilerle, adyabatik süreçte üretilen entalpi değişimi gibi hesaplamalar yapılabilir.
Kalorimetre ve termometre arasındaki fark
Kalorimetre ile termometre arasındaki fark, ölçtükleri termal miktardır. Kazanılan veya kaybedilen ısı miktarını ölçmek için kalorimetre kullanılırken, bir vücudun sıcaklığını ölçmek için termometre kullanılır.
Kalorimetre ve termometre termodinamik deneylerde yaygın olarak kullanılan araçlardır. Aslında bir kalorimetre, içindeki sıcaklığı belirlemek için bir termometreyi entegre eder.