In dit artikel wordt uitgelegd wat een calorimeter is en waarvoor deze wordt gebruikt. Daarnaast ontdek je welke verschillende soorten calorimeters er bestaan en hoe dit meetinstrument werkt.
Wat is een calorimeter?
Een calorimeter is een laboratoriuminstrument dat wordt gebruikt om de hoeveelheid warmte te meten die een lichaam ontvangt of verliest. Bovendien is de calorimeter een instrument dat wordt gebruikt om de soortelijke warmte van een stof te bepalen.
Een calorimeter kan bijvoorbeeld worden gebruikt om energie te meten in de vorm van warmte die vrijkomt tijdens een chemische reactie.
De modernste calorimeters kunnen werken in een breed temperatuurbereik, sommige kunnen 3500 K bereiken. Bovendien zijn de calorimeters momenteel zeer nauwkeurig, ze kunnen een nauwkeurigheid hebben van minder dan 1%, hoewel dit afhankelijk is van de kenmerken en de gebruik van de calorimeter.
Bij calorimetrie zijn de toepassingen van de calorimeter talrijk. Calorimeters kunnen worden gebruikt om een biologisch onderzoek uit te voeren, kwaliteitscontrole uit te voeren of zelfs de biologische snelheid te onderzoeken.
Onderdelen van een calorimeter
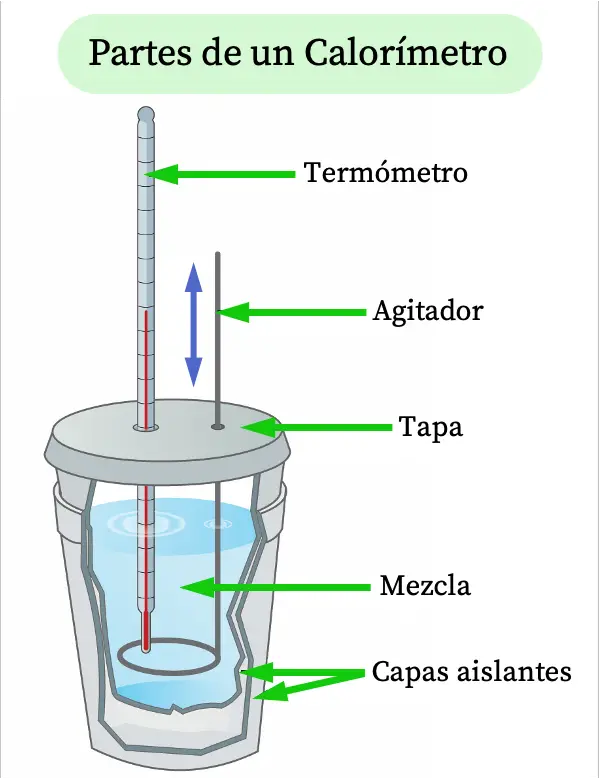
Gezien de definitie van een calorimeter, worden de onderdelen van een typische calorimeter hieronder uitgelegd:
- Thermometer : hiermee kunt u de temperatuur in de calorimeter meten.
- Roerder : onderdeel van de calorimeter dat continu wordt geroerd om de temperatuur van het mengsel te verhogen.
- Deksel : deksel dat geopend en gesloten kan worden om het te onderzoeken mengsel in te brengen.
- Mengsel : dit is de stof waarvoor we een calorische analyse willen uitvoeren.
- Isolatielagen : de calorimetercontainer moet het mengsel thermisch isoleren van buitenaf, zodat de omgevingstemperatuur hier geen invloed op heeft. Daarom bestaan ze doorgaans uit twee lagen thermische isolatie, meestal polystyreen.
Soorten caloriemeters
De verschillende soorten calorimeters zijn als volgt:
- Adiabatische calorimeter : Adiabatische calorimeters worden gebruikt om geïsoleerde adiabatische reacties te bestuderen, dat wil zeggen dat er geen warmte-uitwisseling met de buitenwereld kan plaatsvinden. Er gaat echter altijd een bepaalde hoeveelheid warmte verloren, dus ter compensatie wordt meestal een correctiefactor toegepast.
- Reactiecalorimeter – Er vindt een chemisch proces plaats in de calorimeter, die gesloten en geïsoleerd is. Over het algemeen wordt het gebruikt om de warmte te bepalen die vrijkomt bij een reactie; het wordt ook gebruikt bij reacties waarbij een constante temperatuur vereist is.
- Heat Flux Calorimeter – Bij dit type regelt een verwarmings-/koelmantel de temperatuur van het fysieke proces. De reactiewarmte wordt bepaald door het temperatuurverschil tussen de warmteoverdrachtsvloeistof en de procesvloeistof te meten. Ze zijn minder nauwkeurig dan andere soorten calorimeters.
- Warmtebalanscalorimeter : Dit type calorimeter vereist ook een verwarmings-/koelmantel om de procestemperatuur te regelen. Warmte wordt gemeten door de warmte te monitoren die wordt gewonnen of verloren door de overdrachtsvloeistof.
- Energiegecompenseerde calorimeter : In dit geval wordt een aan de container toegevoegd verwarmingselement gebruikt om een constante temperatuur te handhaven. De verwarmingsenergie kan worden aangepast aan de behoeften van de reactie.
- Calorimeter met constante stroom – Dit type calorimeter zorgt voor een constante warmtestroom door de wand van de container.
- Bomcalorimeter : Dit type calorimeter wordt gebruikt om de verbrandingswarmte te berekenen. Het is gebruikelijk dat een elektrische vonk wordt toegepast om de brandstof te ontsteken. Bovendien werken ze onder zeer hoge druk.
- Calvet-type calorimeter : deze calorimeters maken gebruik van een 3D-flowsensor. Ze zijn zeer geschikt voor grote monsters, omdat ze het gebruik van een groter reactievat mogelijk maken.
- Calorimeter met constante druk : Dit type calorimeter wordt gebruikt om de warmteverandering in een oplossing onder constante druk te meten.
- Differentiële scancalorimeter – Er zijn gewoonlijk twee trays: een monstertray en een referentietray. De monsterbak bevat het monster terwijl de referentiebak leeg blijft. Elke container wordt afzonderlijk met een bepaalde snelheid verwarmd, en deze snelheid wordt gedurende het hele experiment gehandhaafd. Een computersysteem zorgt er echter voor dat elke pan even snel opwarmt, zodat er een meting kan worden gedaan. De heater onder de monstertray moet harder werken dan de lege referentietray en produceert daardoor meer warmte. De calorimeter voert dus de meting uit op basis van het verschil in de hoeveelheid warmte die in de bakken wordt afgegeven.
- Isothermische titratiecalorimeter – Bij dit type wordt de reactiewarmte gebruikt om een titratie-experiment te volgen. Het is mogelijk om het middelpunt van de reactie, de enthalpie en de bindingsaffiniteit ervan te bepalen. Dit type calorimeter is zeer nuttig in de farmaceutische industrie om potentiële kandidaat-geneesmiddelen te classificeren.
Hoe een calorimeter werkt
Zoals je in het vorige gedeelte hebt gezien, zijn er veel soorten calorimeters, dus ze werken allemaal anders. Hieronder wordt uitgelegd hoe de adiabatische calorimeter wordt gebruikt, aangezien deze het meest wordt gebruikt in laboratoriumexperimenten.
De werking van de calorimeter sluit aan op het schudden van de shaker. Voordat u de schudder gebruikt, is het logisch om het monster in de calorimeter te plaatsen. En zodra het deksel gesloten is om het monster te isoleren, moet de roerder snel verplaatst worden, waardoor de temperatuur van het monster zal stijgen. Met de thermometer kun je zien op welke temperatuur het monster zich bevindt.
Vervolgens worden, na het schudden van het monster, de relevante metingen uitgevoerd. Zodat de resultaten kunnen worden vergeleken met de gemeten gegevens voordat het monster wordt verwarmd. En met alle gegevens die tijdens het experiment zijn verzameld, kunnen berekeningen worden gemaakt, zoals de enthalpieverandering die tijdens het adiabatische proces wordt geproduceerd.
Het verschil tussen een calorimeter en een thermometer
Het verschil tussen een calorimeter en een thermometer is de thermische hoeveelheid die ze meten. Een calorimeter wordt gebruikt om de hoeveelheid gewonnen of verloren warmte te meten, terwijl een thermometer wordt gebruikt om de temperatuur van een lichaam te meten.
De calorimeter en thermometer zijn veelgebruikte instrumenten bij thermodynamische experimenten. In feite integreert een calorimeter een thermometer om de temperatuur binnenin te bepalen.