In diesem Artikel wird erklärt, was ein Kalorimeter ist und wofür es verwendet wird. Darüber hinaus erfahren Sie, welche verschiedenen Arten von Kalorimetern es gibt und wie dieses Messgerät funktioniert.
Was ist ein Kalorimeter?
Ein Kalorimeter ist ein Laborinstrument, mit dem die von einem Körper aufgenommene oder verlorene Wärmemenge gemessen wird. Darüber hinaus ist das Kalorimeter ein Instrument zur Bestimmung der spezifischen Wärme einer Substanz.
Mit einem Kalorimeter kann beispielsweise Energie in Form von Wärme gemessen werden, die bei einer chemischen Reaktion freigesetzt wird.
Die modernsten Kalorimeter sind in der Lage, in einem weiten Temperaturbereich zu arbeiten, einige können 3500 K erreichen. Darüber hinaus sind die Kalorimeter derzeit sehr präzise, sie können eine Genauigkeit von weniger als 1 % haben, obwohl dies von den Eigenschaften und der Umgebung abhängt Verwendung des Kalorimeters.
In der Kalorimetrie gibt es zahlreiche Einsatzmöglichkeiten des Kalorimeters. Kalorimeter können zur Durchführung einer biologischen Studie, zur Qualitätskontrolle oder sogar zur Untersuchung der biologischen Rate eingesetzt werden.
Teile eines Kalorimeters
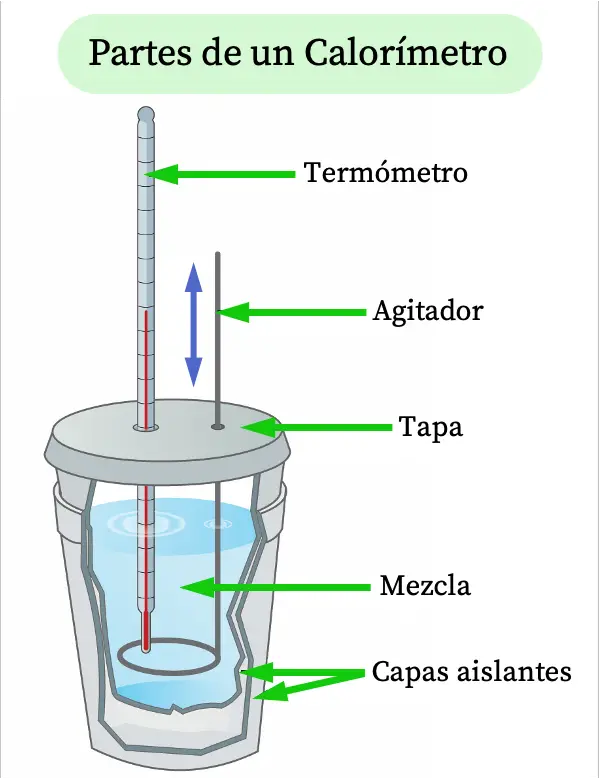
Unter Berücksichtigung der Definition eines Kalorimeters werden im Folgenden die Bestandteile eines typischen Kalorimeters erläutert:
- Thermometer : Ermöglicht die Messung der Temperatur im Kalorimeter.
- Rührer : Teil des Kalorimeters, der kontinuierlich gerührt wird, um die Temperatur der Mischung zu erhöhen.
- Deckel : Deckel, der geöffnet und geschlossen werden kann, um die zu untersuchende Mischung einzuführen.
- Gemisch : Dies ist der Stoff, für den wir eine Kalorienanalyse durchführen möchten.
- Isolierschichten : Der Kalorimeterbehälter muss das Gemisch nach außen thermisch isolieren, damit die Umgebungstemperatur keinen Einfluss darauf hat. Deshalb bestehen sie in der Regel aus zwei Lagen Wärmedämmung, meist Polystyrol.
Arten von Kalorimetern
Die verschiedenen Arten von Kalorimetern sind wie folgt:
- Adiabatisches Kalorimeter : Adiabatische Kalorimeter werden zur Untersuchung isolierter adiabatischer Reaktionen verwendet, das heißt, es kann kein Wärmeaustausch mit der Außenwelt stattfinden. Da jedoch immer eine gewisse Wärmemenge verloren geht, wird zum Ausgleich üblicherweise ein Korrekturfaktor angewendet.
- Reaktionskalorimeter – Im geschlossenen und isolierten Kalorimeter findet ein chemischer Prozess statt. Im Allgemeinen dient es zur Bestimmung der bei einer Reaktion freigesetzten Wärme; Es wird auch bei Reaktionen verwendet, die eine konstante Temperatur erfordern.
- Wärmeflusskalorimeter – Bei diesem Typ regelt ein Heiz-/Kühlmantel die Temperatur des physikalischen Prozesses. Die Reaktionswärme wird durch Messung der Temperaturdifferenz zwischen der Wärmeträgerflüssigkeit und der Prozessflüssigkeit bestimmt. Sie sind weniger präzise als andere Arten von Kalorimetern.
- Wärmebilanzkalorimeter : Dieser Kalorimetertyp erfordert außerdem einen Heiz-/Kühlmantel zur Steuerung der Prozesstemperatur. Die Wärmemessung erfolgt durch Überwachung der von der Übertragungsflüssigkeit gewonnenen oder verlorenen Wärme.
- Energiekompensiertes Kalorimeter : In diesem Fall wird eine dem Behälter hinzugefügte Heizung verwendet, um eine konstante Temperatur aufrechtzuerhalten. Die Heizenergie kann je nach Bedarf der Reaktion angepasst werden.
- Konstantflusskalorimeter – Dieser Kalorimetertyp sorgt für einen konstanten Wärmefluss durch die Wand des Behälters.
- Bombenkalorimeter : Dieser Kalorimetertyp wird zur Berechnung der Verbrennungswärme verwendet. Es ist üblich, dass zur Zündung des Kraftstoffs ein elektrischer Funke angelegt wird. Darüber hinaus arbeiten sie mit sehr hohen Drücken.
- Calvet-Kalorimeter : Diese Kalorimeter verwenden einen 3D-Durchflusssensor. Sie eignen sich gut für große Probenmengen, da sie die Verwendung eines größeren Reaktionsgefäßes ermöglichen.
- Konstantdruckkalorimeter : Dieser Kalorimetertyp wird verwendet, um die Wärmeänderung in einer Lösung unter konstantem Druck zu messen.
- Dynamisches Differenzkalorimeter – Normalerweise gibt es zwei Tabletts, ein Probentablett und ein Referenztablett. Das Probentablett enthält die Probe, während das Referenztablett leer bleibt. Jeder Behälter wird separat mit einer bestimmten Geschwindigkeit erhitzt und diese Geschwindigkeit wird während des gesamten Experiments beibehalten. Ein Computersystem stellt jedoch sicher, dass jede Pfanne mit der gleichen Geschwindigkeit erhitzt wird, sodass eine Messung durchgeführt werden kann. Die Heizung unter dem Probentablett muss stärker arbeiten als das leere Referenztablett und erzeugt daher mehr Wärme. Somit führt das Kalorimeter die Messung entsprechend der Differenz der in den Schalen abgegebenen Wärmemenge durch.
- Isothermes Titrationskalorimeter – Bei diesem Typ wird die Reaktionswärme zur Überwachung eines Titrationsexperiments verwendet. Es ist möglich, den Mittelpunkt der Reaktion, ihre Enthalpie und ihre Bindungsaffinität zu bestimmen. Diese Art von Kalorimeter ist in der Pharmaindustrie sehr nützlich, um potenzielle Arzneimittelkandidaten zu klassifizieren.
Wie ein Kalorimeter funktioniert
Wie Sie im vorherigen Abschnitt gesehen haben, gibt es viele Arten von Kalorimetern, sodass jedes anders funktioniert. Im Folgenden wird die Verwendung des adiabatischen Kalorimeters erläutert, da es in Laborexperimenten am häufigsten verwendet wird.
Der Betrieb des Kalorimeters erfolgt durch Schütteln des Schüttlers. Vor der Verwendung des Schüttlers ist es sinnvoll, die Probe in das Kalorimeter einzuführen. Und sobald der Deckel geschlossen ist, um die Probe zu isolieren, muss der Rührer schnell bewegt werden, wodurch die Temperatur der Probe ansteigt. Mit dem Thermometer können Sie sehen, welche Temperatur die Probe hat.
Anschließend werden nach dem Schütteln der Probe die entsprechenden Messungen durchgeführt. Damit die Ergebnisse vor dem Erhitzen der Probe mit den Messdaten verglichen werden können. Und mit allen während des Experiments gesammelten Daten können Berechnungen durchgeführt werden, beispielsweise zur Enthalpieänderung, die beim adiabatischen Prozess entsteht.
Unterschied zwischen einem Kalorimeter und einem Thermometer
Der Unterschied zwischen einem Kalorimeter und einem Thermometer besteht in der thermischen Größe, die sie messen. Mit einem Kalorimeter wird die aufgenommene oder verlorene Wärmemenge gemessen, während mit einem Thermometer die Körpertemperatur gemessen wird.
Kalorimeter und Thermometer sind gängige Instrumente in thermodynamischen Experimenten. Tatsächlich ist in ein Kalorimeter ein Thermometer integriert, um die Innentemperatur zu bestimmen.